
佐藤 かお理 先生の紹介
略歴
平成18年 3月 東京学芸大学 教育学部 初等教育教員養成課程 理科選修 卒業 (東京学芸大学 生命科学:吉野 正巳 教授) 平成18年 4月 総合研究大学院大学 生命科学研究科・生理科学専攻 5年一貫博士課程 入学 平成23年 3月 総合研究大学院大学 5年一貫博士課程 終了 (生理学研究所 機能協関部門:岡田 泰伸 教授) 平成23年 4月 自然科学研究機構・生理学研究所・NIPSリサーチフェロー (生理学研究所・機能協関部門:岡田 泰伸 教授) 平成26年 8月 自然科学研究機構・生理学研究所・研究員 (生理学研究所・細胞生理部門:富永 真琴 教授) 平成27年 4月 日本学術振興会・特別研究員(RPD) (福岡大学・医学部・生理学講座:井上 隆司 教授) 令和4年 1月 秋田大学大学院医学系研究科 助教 (秋田大学・大学院医学系研究科・器官・統合生理学講座:沼田 朋大 教授)
研究テーマ
その1:『バソプレシンニューロンの容積調節メカニズムの解明とバソプレシンの軸索分泌制御メカニズムの解明』
『バソプレシンとは?』
バソプレシン(アルギニンバソプレシン:AVP)とは、抗利尿ホルモンとして知られている、尿の量を調節するホルモンです。 夏の暑いときに、室内や屋外で活動していると脱水が起こります。私たちのからだでは、体内の水分の減少を脳で感知してAVPを分泌することが知られています。血液中に分泌されたAVPは、腎臓に働きかけて体内への水の再吸収を促し、体の外に出す尿の量を減らすことで体内の水分量を維持します。一方、水の一気飲みなどで、体内の水分量が急激に増えると、血中のAVPが減少します。血中AVPの減少により、腎臓で水の再吸収が抑えられると、尿が出て、体内の水分量を維持します。


『バソプレシンニューロンの容積調節メカニズムの解明』
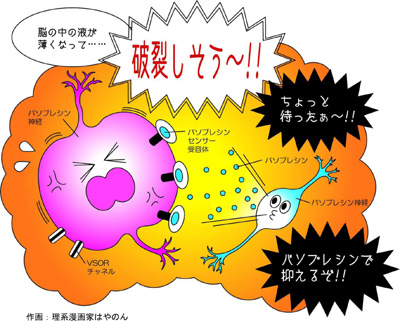
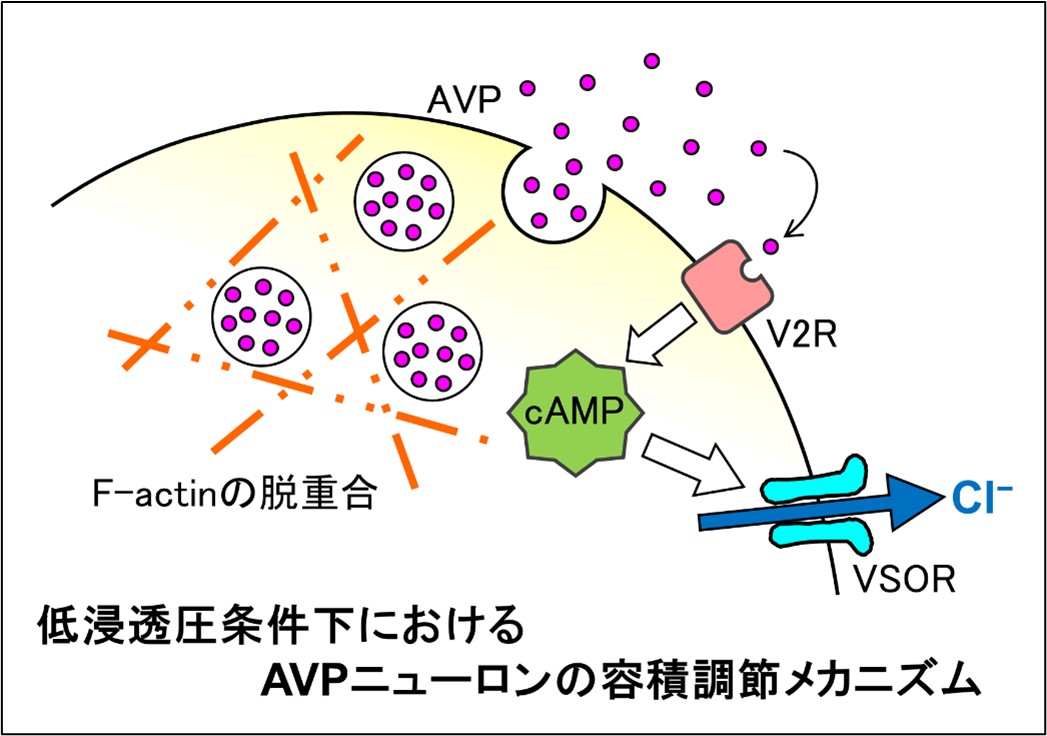
バソプレシン(AVP)は、のどの渇きなどで血中の浸透圧が上昇すると、脳・視床下部にあるAVP産生ニューロンで作られ、脳下垂体後葉から血中に分泌されます。そのため、AVP産生ニューロンは、体内水分量の恒常性を維持する中心的な役割を担っていると考えられています。 多くの動物細胞は、体液の浸透圧が上昇すると細胞が縮小し、低い浸透圧になると膨張します。細胞容積の持続的な縮小・膨張は、細胞死を引き起こす原因となるため、細胞の大きさを一定に維持するために細胞容積を調節する機能を持っています。 これまで、AVP産生ニューロンは細胞容積を調節する機能がないという報告がされてきました(Zhang et al. 2003 Nat Neurosci)。しかし、多くの動物細胞が有する細胞容積調節能は、細胞生存において必要不可欠な要素であるため、この機能がないというのはAVP産生ニューロンにとって細胞の生存にも影響するのではないか、という疑問が起こります。 この問題について解決するために私たちは、AVP産生ニューロンのみを識別できる特別な細胞を用いて、研究を行ってきました。この継続的な研究の結果、AVP産生ニューロンにも細胞容積を調節する能力があり、他の動物細胞種と同様に、AVP ニューロンの膜に発現しているVSOR が深く関与している事を明らかにしました。更に、体液中の水分量が増加するする低浸透圧刺激では、軸索終末からのAVP 分泌は抑制されるのに反してAVPニューロンの細胞体・樹状突起からのAVP の開口分泌が増えることを見出し、そのメカニズムは、低浸透圧による細胞骨格・F-アクチンの脱重合によるものである事を明らかにしました。このAVP は、AVP ニューロンに発現しているV2 型AVP レセプター(V2R)を刺激して、cAMP を介し、細胞の容積調節に重要な役割を担うことが知られている塩化物イオンチャネル(VSOR) の活性を更に亢進し、浸透圧性膨張後の容積回復を更に促進するというポジティブフィードバックメカニズムを明らかにしました(図参照;Sato et al. Science Signaling 2011)。 現在は、体液中の水分量が減少する高浸透圧条件下におけるAVP産生ニューロンの容積調節メカニズムについて研究を進めています。
『バソプレシンの軸索分泌制御メカニズムの解明』
バソプレシン(AVP)は、体液中の水分量が増えると血中への分泌量が増え、減少すると分泌量が減ることが広く知られています。 体液中の水分量が増える低浸透圧条件下で分泌量が減るメカニズムは、AVP産生ニューロンの近傍にあるグリア細胞からタウリンという物質が分泌され、それがAVP産生ニューロンに作用すると、AVP産生ニューロンの膜が過分極を起して軸索終末から血中へ分泌されるAVP量が減るというストーリーが教科書的定説として知られています。しかし、2014年に、AVP産生ニューロンにタウリンが作用すると過分極ではなく『脱分極』する、という新事実が報告されました(Haam et al. 2012 J Neurosci)。この新事実は、これまでの定説が矛盾していることを意味しており、低浸透圧条件下における軸索AVP分泌制御メカニズムを根本的に再検討する必要が生じてきています。私は、この矛盾に挑み、タウリンがどのようにして血中に分泌されるAVP量を抑制しているのかについて研究を進めています。
その2:『酸感受性アニオンチャネルの生理機能の解明』
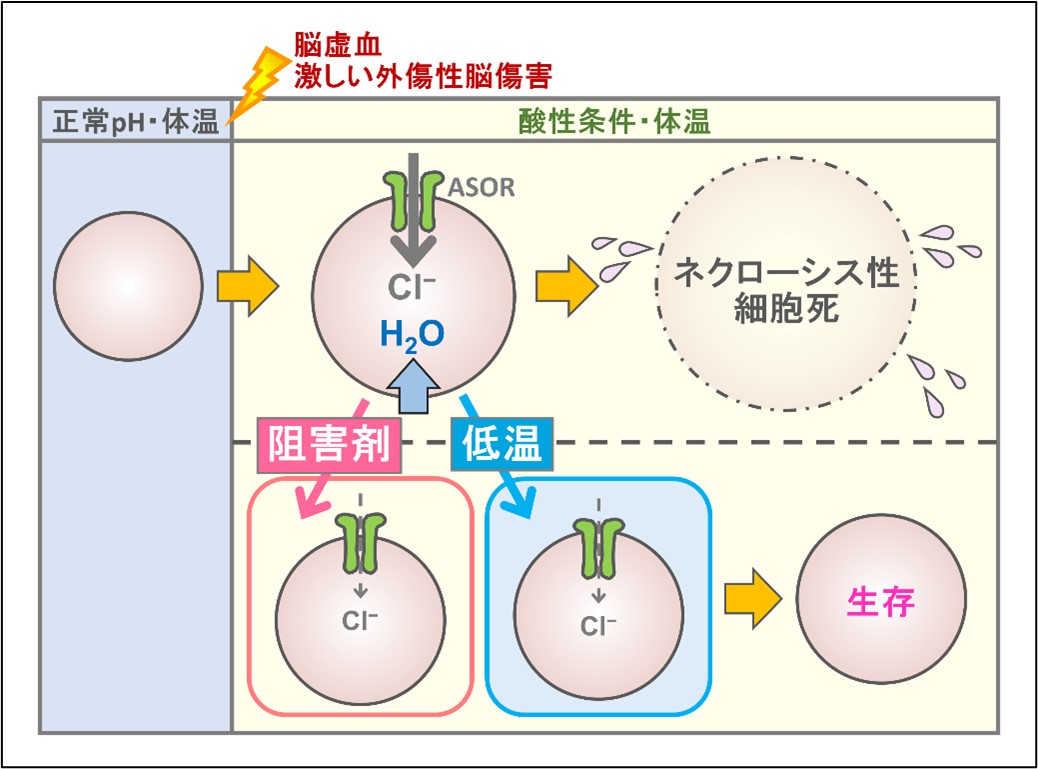
酸感受性外向整流性アニオンチャネルASOR(acid-sensitive outwardly rectifying anion channel)は、2003年にセルトリ細胞で初めて発見された(Auzanneau et al, J Biol Chem, 2003)酸で活性化する塩化物イオンチャネルで、その後の研究により様々な細胞種に発現していることが報告されています(Yamamoto et al, Am J Physiol Heart Circ Physiol, 2006; Wang et al, Pflügers Arch, 2006, Sato-Numata et al, Channels, 2014)。 私たちの研究グループは、ASORの生理的役割について研究を進めており、これまでに1. ASORは外傷により二次的に引き起こされる強度のアシドーシス条件下で活性化し、細胞を膨張させてネクローシス性細胞死を引き起こす事(Wang et al, Pflügers Arch, 2006)、2. 子宮頸癌由来HeLa細胞に発現するASORに温度感受性があり、体温に近い温度で活性が増大する事(Sato-Numata et al, Pflügers Arch, 2013)、3. マウスの大脳皮質神経細胞にもASORが発現しており、脳虚血や外傷によって脳神経が受けるネクローシス性細胞死は、ASORの低温性抑制によって抑制される事(Sato-Numata et al, Channels, 2014)などを明らかにしました。 現在、私たちの研究グループでは、ASORの生理的な役割を明らかにするとともに薬理学的性質についても研究を進めています。
研究業績
科研費取得状況
https://kaken.nii.ac.jp/d/r/60614196.ja.html
資格・免許
小学校教諭1種免許(平成18年: 東京都教育委員会) 中学校教諭1種免許(理科)(平成18年: 東京都教育委員会) 高等校教諭1種免許(理科)(平成18年: 東京都教育委員会) 理学博士号 (平成23年: 総合研究大学院大学)
賞罰
日本生理学会九州奨励賞(平成27年:西日本生理学会) 入澤宏・彩記念若手研究奨励賞(平成29年:日本生理学会)
趣味
料理、観光地めぐり、各地の珍しい食材探し
