研究の公開研究内容業績
消化管分野
基礎的研究および県内外の関連病院とも連携して各種臨床研究を行っています。
<研究の一例>
- 食道腺癌の動向に関する疫学調査
- 難治性潰瘍に対するボノプラザンの有効性についての検討
- 特発性潰瘍の病態と治療
- ヘリコバクター・ピロリ除菌後胃癌におけるアセトアルデヒド脱水素酵素遺伝子多型について
- バレット食道の発癌リスクに関する検討
- バレット腺癌、食道胃接合部癌と肥満との関連について
- 消化管出血症例における予後不良因子の検討
- 画像強調内視鏡の食道扁平上皮癌検出能に関する多施設共同ランダム化比較試験など
炎症性腸疾患分野
秋田県内の関連施設と協力し潰瘍性大腸炎、クローン病の患者さんの役に立つ実臨床に即した研究、特に患者さんの長期経過の改善につながる薬剤使用や内視鏡的評価の改良に関する研究などを行っています。
腸管は最大の免疫臓器であり、摂取した食事やヒトの細胞よりも多いと言われる100兆個もの腸内細菌による影響を常時受けながら全身の免疫をコントロールしています。我々は、腸管のホメオスタシスや腸炎の機序についてサイトカイン、小胞体ストレス、オートファジー、腸内細菌などに関連する様々な基礎的な研究を培養細胞、マウス、ヒト検体などを用い行っています。
肝グループ
患者の保存血清を用いたB型慢性肝炎、C型慢性肝炎、非アルコール性脂肪性肝炎(NASH)等の臨床研究を行っています。
腹部超音波検査時にARFIを測定し、非侵襲的な肝線維化の評価を行い、治療効果予測や治療後の肝線維化改善の経時的変化を検討しています。また、肝腫瘍の診断へのARFIの応用を検討しています。
関連病院と協力し、秋田県の肝疾患の特徴についての疫学的検討や、最近の肝炎治療の有効性の検討を行っています。
肝疾患基礎研究グループ
現在、遺伝子改変マウスなどの動物モデルを使用し、NAFLD、肝線維化、肝発癌の研究を行っています。肝疾患と自然免疫機構との関連に注目し、特に肝疾患におけるToll-like受容体や腸内細菌の役割などを解析しています。消化器疾患と免疫は一見関連ない分野に思えますが、摂取する食事や肥満状態でも自然免疫機構に変化を来たし、それが長年続くと少なからず肝疾患に影響を及ぼすことが判明しつつあります。B型慢性肝炎やC型慢性肝炎は肝硬変や肝癌を来す代表的肝疾患ですが、糖尿病や肥満も独立した肝癌の危険因子であることが最近の疫学調査で判明しています。我々のグループでは分子生物学的手法を用いて、それらメカニズムの解明と治療応用に向けた検討を行っています。いくつかの成果は国際学会での発表のみならず、海外の一流ジャーナルに掲載されています。今後、これらの成果をいかに臨床に応用するか模索しているところです。また一部研究では国内外の第一線の研究室との共同研究を行い、世界の最新情報を入手しつつ研究を行っています。
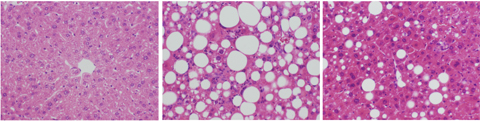
最近の主なpublication
Miura K et al.
Gastroenterology 2010:139;323-34
Miura K et al. Am J Physiol Gastrointest Liver Physiol. 2012 ;302:G1310-21.
Miura K et al. Hepatology 2013;57:577-89
神経内科学分野
神経内科のあつかう領域は、‘治らない病気が多い’と受け取られがちですが、近年の驚くべき神経科学の進歩は明るい光を投げかけています。原因遺伝子が同定され、病態に基づく治療薬の登場がそう遠くない疾患もでてきています。
私たちも、以下のようなテーマを加え、十分な治療法がいまだ確立していない、いわゆる神経難病の病態解明にかかわる研究をしています。
今後の神経科学の輝かしい将来とともに歩むことができるのも、神経内科の魅力のひとつと思います。
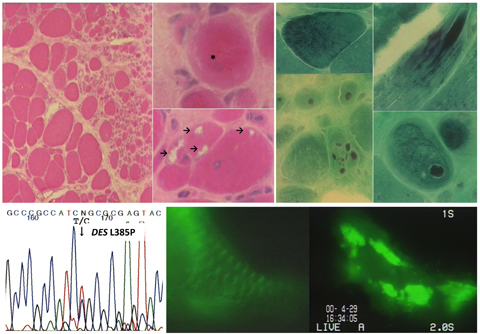
- 分子モーターとモーター関連たんぱくの研究
- 中間径フィラメントたんぱくの研究
- 筋萎縮性側索硬化症の病因解明
- 脊髄小脳変性症、筋疾患の遺伝子診断
- ジストニアの臨床研究、ボツリヌス毒素治療
- 神経難病の療養環境整備(地域医療体制の構築に関する研究)
- 痴呆を伴う筋萎縮性側索硬化症の臨床的研究
- 前頭側頭型痴呆の臨床的研究
- 神経免疫疾患の治療研究